Korozja elektrochemiczna: niszczenie metali wskutek reakcji chemicznych i prądów elektrycznych
- Korozja elektrochemiczna to proces degradacji metali wymagający anody, katody i elektrolitu.
- Jej mechanizm opiera się na tworzeniu mikroogniw galwanicznych na powierzchni metalu.
- Szybkość korozji przyspieszają wilgoć, tlen, sole, temperatura oraz zanieczyszczenia środowiska.
- Wyróżnia się różne typy korozji, np. wżerową, szczelinową czy galwaniczną, każda z własną charakterystyką.
- Skuteczne metody ochrony obejmują powłoki ochronne, ochronę katodową i anodową oraz inhibitory.
- Zjawisko to jest powszechne w samochodach, instalacjach domowych i konstrukcjach stalowych.
Czym jest korozja i dlaczego jej elektrochemiczna odmiana jest wszechobecna?
Korozja elektrochemiczna to proces niszczenia metali, który zachodzi w wyniku działania mikroogniw galwanicznych na ich powierzchni, w obecności elektrolitu. Można ją zdefiniować jako samorzutne niszczenie materiałów pod wpływem oddziaływania środowiska. Jest to zjawisko wszechobecne w naszym otoczeniu, ponieważ metale, dążąc do stanu niższego energetycznie, reagują z otoczeniem, powracając do formy bardziej stabilnej, często przypominającej rudy, z których zostały wydobyte. Widzimy ją na zardzewiałych elementach samochodów, w instalacjach wodnych, a nawet na biżuterii.Do zaistnienia korozji elektrochemicznej niezbędne są trzy kluczowe elementy, które tworzą miniaturowe ogniwo galwaniczne. Po pierwsze, potrzebna jest anoda, czyli obszar metalu, który ulega utlenianiu i rozpuszczaniu. To właśnie tutaj metal oddaje elektrony i przechodzi do roztworu w postaci jonów. Po drugie, konieczna jest katoda – obszar, na którym zachodzi redukcja substancji zwanej depolaryzatorem, najczęściej tlenu lub jonów wodorowych. Katoda przyjmuje elektrony uwolnione na anodzie. Trzecim, równie ważnym składnikiem jest elektrolit, czyli środowisko przewodzące prąd elektryczny, które umożliwia przepływ jonów między anodą a katodą. Najczęściej jest to woda zawierająca rozpuszczone sole, kwasy lub zasady.
Warto odróżnić korozję elektrochemiczną od chemicznej. Korozja chemiczna, jak sama nazwa wskazuje, polega na bezpośredniej reakcji metalu ze środowiskiem, bez udziału prądów elektrycznych, np. utlenianie metalu w wysokiej temperaturze. Natomiast w korozji elektrochemicznej kluczową rolę odgrywa przepływ elektronów i jonów, co czyni ją znacznie bardziej złożonym i często szybciej postępującym procesem.
Jak w praktyce przebiega niewidzialny proces niszczenia metalu?
Zrozumienie mechanizmu korozji elektrochemicznej pozwala nam lepiej walczyć z jej skutkami. Cały proces rozpoczyna się na powierzchni metalu, gdzie tworzą się mikroogniwa galwaniczne. Na obszarze metalu o niższym potencjale elektrochemicznym, zwanym anodą, dochodzi do utleniania, czyli rozpuszczania metalu. Przykładowo, w przypadku żelaza, atom żelaza oddaje elektrony i przechodzi do roztworu jako jon: Fe → Fe²⁺ + 2e⁻. Te uwolnione elektrony migrują przez metal do obszaru o wyższym potencjale, czyli do katody.
Na katodzie następuje redukcja tak zwanego depolaryzatora. W zależności od środowiska, wyróżniamy dwa główne scenariusze ataku:
- Depolaryzacja tlenowa: W środowisku obojętnym lub zasadowym, a także w obecności tlenu (co jest bardzo powszechne), depolaryzatorem jest tlen rozpuszczony w wodzie. Reakcja na katodzie wygląda następująco: O₂ + 2H₂O + 4e⁻ → 4OH⁻. W ten sposób powstają jony wodorotlenkowe.
- Depolaryzacja wodorowa: W środowisku kwaśnym, depolaryzatorem są jony wodorowe. Reakcja katodowa to: 2H⁺ + 2e⁻ → H₂. W tym przypadku wydziela się gazowy wodór.
Powstałe na anodzie jony metalu (np. Fe²⁺) reagują następnie z jonami wodorotlenkowymi (OH⁻) powstałymi na katodzie (w przypadku depolaryzacji tlenowej), tworząc wodorotlenek żelaza. Ten związek, w dalszych reakcjach z tlenem i wodą, przekształca się w hydratowane tlenki żelaza, które znamy jako rdzę (np. Fe₂O₃·nH₂O). Rdza jest porowata i nie stanowi skutecznej bariery ochronnej, co pozwala na dalsze wnikanie tlenu i wody, a tym samym na kontynuację procesu korozji.
Rola potencjału elektrochemicznego jest tu kluczowa. Metale różnią się swoją aktywnością chemiczną, co przekłada się na ich potencjał elektrochemiczny. Im niższy potencjał, tym metal jest bardziej aktywny i łatwiej ulega utlenianiu. Dlatego też, gdy dwa różne metale stykają się w obecności elektrolitu, metal o niższym potencjale "poświęca się" i koroduje szybciej, chroniąc tym samym metal o wyższym potencjale. Jest to podstawa ochrony katodowej, o której opowiem więcej w dalszej części artykułu.
Co decyduje o szybkości rdzewienia? Kluczowe czynniki przyspieszające korozję
Szybkość, z jaką metal ulega korozji elektrochemicznej, zależy od wielu czynników. Zrozumienie ich jest kluczowe dla skutecznej ochrony. Poniżej przedstawiam najważniejsze z nich i ich wpływ na proces degradacji:
| Czynnik | Wpływ na korozję |
|---|---|
| Obecność elektrolitów | Sole, takie jak chlorek sodu (sól drogowa), znacznie zwiększają przewodnictwo elektryczne wody, co przyspiesza przepływ jonów i elektronów w ogniwach korozyjnych. Im wyższe stężenie elektrolitu, tym szybciej zachodzi korozja. |
| Wilgotność i tlen | Są to niezbędne składniki do utworzenia ogniwa korozyjnego. Wilgoć działa jako elektrolit, a tlen jest depolaryzatorem. Bez choćby jednego z nich korozja elektrochemiczna nie może zajść. Wysoka wilgotność powietrza i kontakt z wodą znacząco przyspieszają proces. |
| Temperatura | Wyższa temperatura zazwyczaj zwiększa szybkość reakcji chemicznych, w tym procesów korozyjnych. Wzrost temperatury przyspiesza dyfuzję tlenu i jonów, a także zwiększa przewodnictwo elektrolitu. |
| Zanieczyszczenia powietrza | Tlenki siarki (SO₂) i azotu (NOx) reagują z parą wodną w atmosferze, tworząc kwasy (np. siarkowy, azotowy). Te kwaśne deszcze obniżają pH środowiska, co sprzyja korozji wodorowej i znacząco przyspiesza niszczenie metali, zwłaszcza stali. |
| Styk różnych metali | Kiedy dwa metale o różnym potencjale elektrochemicznym stykają się w obecności elektrolitu, tworzy się ogniwo galwaniczne. Metal mniej szlachetny (o niższym potencjale) staje się anodą i ulega przyspieszonej korozji, chroniąc metal bardziej szlachetny. To zjawisko nazywamy korozją galwaniczną. |
| Naprężenia i uszkodzenia mechaniczne | Zarysowania, pęknięcia, wygięcia czy inne uszkodzenia mechaniczne tworzą na powierzchni metalu obszary o zmienionej strukturze krystalicznej i wyższym potencjale energetycznym. Te miejsca stają się preferencyjnymi anodami, inicjując i przyspieszając korozję. |
Jak widać, wiele z tych czynników jest ze sobą powiązanych i często występują jednocześnie, potęgując wzajemnie swoje działanie. Dlatego tak ważne jest kompleksowe podejście do problemu ochrony przed korozją.
Najgroźniejsze oblicza korozji – jakie typy wyróżniamy i jak je rozpoznać?
Korozja elektrochemiczna to nie jednolity proces. W zależności od warunków i materiału może przyjmować różne formy, każda z własną charakterystyką i potencjalnymi zagrożeniami. Rozpoznanie typu korozji jest kluczowe do wyboru odpowiedniej metody ochrony.
Korozja galwaniczna (stykowa): Ten typ korozji występuje, gdy dwa różne metale stykają się ze sobą w obecności elektrolitu. Metal o niższym potencjale elektrochemicznym (mniej szlachetny) działa jako anoda i ulega przyspieszonemu niszczeniu, podczas gdy metal bardziej szlachetny jest chroniony. Klasycznym przykładem jest połączenie stali z miedzią w instalacji wodnej – stal będzie korodować szybciej. Jak podaje Wikipedia, korozja galwaniczna jest jednym z najczęściej spotykanych typów korozji w przemyśle.Korozja wżerowa: Jest to szczególnie niebezpieczna forma korozji, która prowadzi do powstawania głębokich, punktowych ubytków, czyli wżerów, na powierzchni metalu. Często rozwija się pod warstwą produktów korozji, co utrudnia jej wczesne wykrycie. Jest typowa dla stali nierdzewnych i aluminium w obecności jonów chlorkowych (np. w wodzie morskiej). Wżery mogą prowadzić do perforacji materiału, nawet jeśli ogólna utrata masy jest niewielka.
Korozja szczelinowa: Atakuje metale w ciasnych przestrzeniach, szczelinach, pod uszczelkami, nitami czy śrubami, gdzie dostęp tlenu jest ograniczony. W tych miejscach tworzą się różnice w stężeniu tlenu, co prowadzi do powstania ogniw korozyjnych. Obszary o niższym stężeniu tlenu stają się anodami i ulegają korozji. Jest to problematyczne w konstrukcjach spawanych i łączonych.
Korozja równomierna: To najbardziej powszechny, ale zarazem najmniej groźny typ korozji, ponieważ atakuje całą powierzchnię metalu w sposób jednolity. Chociaż prowadzi do stopniowej utraty materiału, jest stosunkowo łatwa do przewidzenia i kontrolowania. Przykładem jest równomierne rdzewienie stali węglowej w wilgotnym powietrzu.
Korozja międzykrystaliczna: Ten typ korozji atakuje metal wzdłuż granic ziaren, czyli obszarów, gdzie stykają się ze sobą różne orientacje krystaliczne materiału. Często jest niewidoczna na powierzchni, ale może prowadzić do znacznego osłabienia struktury metalu, a nawet jego pęknięcia. Jest typowa dla niektórych stopów, np. stali nierdzewnych, po obróbce cieplnej, która prowadzi do wydzielania się węglików chromu na granicach ziaren.
Korozja naprężeniowa: Jest to połączenie działania naprężeń mechanicznych (rozciągających) i środowiska korozyjnego. Metal poddany jednocześnie obciążeniu i agresywnemu środowisku może pękać, nawet jeśli żadne z tych czynników osobno nie byłoby wystarczające do uszkodzenia. Jest to szczególnie niebezpieczne, ponieważ pęknięcia mogą rozwijać się szybko i bez ostrzeżenia, prowadząc do katastrofalnych awarii.
Każdy z tych typów korozji wymaga specyficznego podejścia w zakresie diagnostyki i zapobiegania, co podkreśla złożoność problemu degradacji materiałów.
Skuteczne strategie obrony: jak chronić metale przed korozją elektrochemiczną?
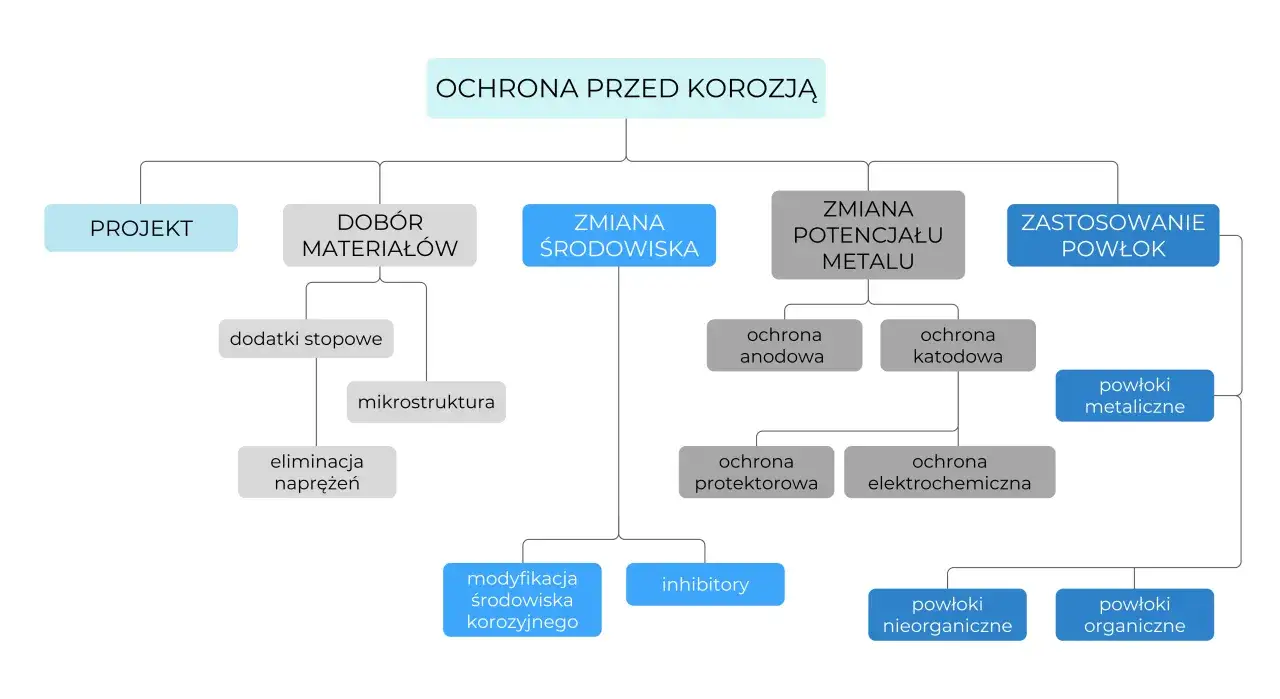
Walka z korozją elektrochemiczną to nieustanne wyzwanie, ale na szczęście dysponujemy szeregiem skutecznych metod ochrony. Ich wybór zależy od rodzaju metalu, środowiska, w którym pracuje, oraz oczekiwanej trwałości. Oto najważniejsze strategie:
-
Powłoki ochronne:
- Niemetaliczne: To najczęściej stosowana i najbardziej widoczna forma ochrony. Powłoki malarskie, lakiernicze czy te wykonane z tworzyw sztucznych (np. epoksydowe, poliuretanowe) tworzą fizyczną barierę, która izoluje metal od agresywnego środowiska (wilgoci, tlenu, substancji chemicznych). Ich skuteczność zależy od szczelności i odporności na uszkodzenia mechaniczne.
-
Metaliczne: Polegają na pokrywaniu chronionego metalu (najczęściej stali) warstwą innego metalu, który jest bardziej odporny na korozję lub pełni funkcję protektorową.
- Cynkowanie: Bardzo popularne, np. w blachach samochodowych czy elementach konstrukcyjnych. Cynk jest metalem mniej szlachetnym niż stal, więc w przypadku uszkodzenia powłoki, to on koroduje (działa jako anoda), chroniąc stal (katodę).
- Chromowanie i niklowanie: Tworzą twarde, błyszczące i odporne na korozję warstwy, często stosowane w celach dekoracyjnych, ale również ochronnych (np. w armaturze łazienkowej, elementach motocyklowych).
-
Ochrona elektrochemiczna: To zaawansowane metody, które aktywnie zmieniają potencjał elektrochemiczny metalu.
-
Ochrona katodowa: Polega na uczynieniu chronionego obiektu katodą ogniwa korozyjnego, co zapobiega jego utlenianiu. Można to osiągnąć na dwa sposoby:
- Poprzez połączenie chronionego obiektu z bardziej aktywnym metalem (tzw. protektorem), który "poświęca się" i koroduje zamiast chronionej konstrukcji (np. cynkowe lub magnezowe anody protektorowe dla kadłubów statków, rurociągów, zbiorników).
- Poprzez podłączenie chronionego obiektu do zewnętrznego źródła prądu stałego, które wymusza przepływ elektronów, czyniąc obiekt katodą.
- Ochrona anodowa: Stosowana dla metali, które ulegają pasywacji, czyli tworzą na swojej powierzchni szczelną, ochronną warstwę tlenków (np. aluminium, stal nierdzewna, tytan). Polega na utrzymywaniu metalu w zakresie potencjałów, w którym tworzy się i utrzymuje ta pasywna warstwa, co znacznie zwiększa jego odporność na korozję.
-
Ochrona katodowa: Polega na uczynieniu chronionego obiektu katodą ogniwa korozyjnego, co zapobiega jego utlenianiu. Można to osiągnąć na dwa sposoby:
- Inhibitory korozji: Są to substancje chemiczne, które dodawane do środowiska (np. do wody w układach chłodzenia, olejów, smarów) w niewielkich stężeniach, znacząco spowalniają procesy korozyjne. Działają poprzez tworzenie ochronnych warstw na powierzchni metalu lub modyfikowanie środowiska.
- Odpowiednie projektowanie: To często niedoceniana, ale fundamentalna metoda. Polega na eliminowaniu czynników sprzyjających korozji już na etapie projektowania konstrukcji. Obejmuje to unikanie kontaktu różnych metali (lub ich izolowanie), eliminowanie szczelin i miejsc, w których może gromadzić się woda lub zanieczyszczenia, a także zapewnienie odpowiedniego drenażu i wentylacji.
Stosując te metody, możemy znacząco wydłużyć żywotność metali i konstrukcji, minimalizując straty wynikające z korozji.
Korozja elektrochemiczna w życiu codziennym – gdzie ją spotkasz i jak z nią walczyć?
Korozja elektrochemiczna nie jest jedynie problemem przemysłowym czy akademickim – otacza nas każdego dnia. Zrozumienie, gdzie i dlaczego występuje, pozwala nam lepiej dbać o nasze mienie.
Rdza na samochodzie: To chyba najbardziej powszechny przykład. Skąd się bierze? Przede wszystkim z soli drogowej używanej zimą, która działa jak doskonały elektrolit, przyspieszając korozję podwozia i nadkoli. Zarysowania i uszkodzenia lakieru (np. od kamieni) odsłaniają metal, tworząc anody i katody. Do tego dochodzi wilgoć, która jest wszechobecna. Aby zapobiegać, kluczowa jest regularna konserwacja podwozia i profili zamkniętych, szybka naprawa wszelkich uszkodzeń lakieru oraz częste mycie samochodu, zwłaszcza zimą, aby usunąć sól.
Instalacje wodne i grzewcze: W naszych domach korozja toczy niewidoczną walkę w rurach. Problem pojawia się, gdy w instalacji stykają się różne metale (np. miedź z elementami stalowymi), tworząc ogniwa galwaniczne. Jakość wody również ma znaczenie – jej twardość, zawartość tlenu czy chlorków wpływa na agresywność środowiska. W systemach grzewczych, gdzie często brakuje tlenu, mogą rozwijać się specyficzne typy korozji. Nowoczesne instalacje stosują materiały odporne na korozję lub systemy ochrony, a także inhibitory dodawane do wody.
Konstrukcje stalowe i mosty: Gigantyczne konstrukcje, takie jak mosty, wiadukty czy maszty, są nieustannie narażone na działanie czynników atmosferycznych. Wilgoć, deszcz, zanieczyszczenia powietrza (tlenki siarki i azotu) tworzą agresywne środowisko. Inżynierowie i konserwatorzy muszą stosować kompleksowe systemy ochrony, w tym grube powłoki malarskie, cynkowanie ogniowe, a w niektórych przypadkach nawet ochronę katodową, aby zapewnić integralność i bezpieczeństwo tych budowli przez dziesięciolecia.
Praktyczne porady dla użytkownika:
- Szybka reakcja: Gdy tylko zauważysz pierwsze ogniska korozji (np. małe pęcherzyki pod lakierem, rdzawy nalot), działaj natychmiast. Im szybciej zareagujesz, tym łatwiej i taniej będzie powstrzymać jej rozprzestrzenianie.
- Czyszczenie i zabezpieczenie: Usuń rdzę mechanicznie lub chemicznie, a następnie zabezpiecz powierzchnię odpowiednim podkładem antykorozyjnym i warstwą ochronną (farbą, lakierem).
- Regularna inspekcja: Sprawdzaj regularnie miejsca szczególnie narażone na korozję, takie jak spawy, zagięcia, miejsca styku różnych materiałów czy obszary poddane uszkodzeniom mechanicznym.
- Unikaj gromadzenia wody: Zadbaj o to, aby woda nie zalegała w trudno dostępnych miejscach, np. w odpływach samochodu czy na elementach ogrodzenia.
Pamiętaj, że zapobieganie jest zawsze lepsze niż leczenie. Dbanie o metale to inwestycja w ich długowieczność i nasze bezpieczeństwo.