Metale to grupa materiałów, które od zarania dziejów kształtowały rozwój cywilizacji, od prostych narzędzi po zaawansowane technologie. Zrozumienie ich natury jest kluczowe, by docenić ich wszechobecność i niezastąpioną rolę w naszym życiu. Ten artykuł dostarczy fundamentalnej wiedzy na temat metali, od ich definicji i budowy, przez kluczowe właściwości, aż po praktyczne zastosowania, odpowiadając na potrzebę kompleksowego zrozumienia tego niezwykłego materiału.
Metale: fundament cywilizacji od rudy po smartfon
- Metale to pierwiastki chemiczne lub ich stopy, stanowiące większość pierwiastków w układzie okresowym.
- Charakteryzują się dobrym przewodnictwem cieplnym i elektrycznym, kowalnością, ciągliwością oraz metalicznym połyskiem.
- Chemicznie metale mają tendencję do oddawania elektronów, tworząc kationy i reagując z kwasami.
- Ich unikalne właściwości wynikają z wiązania metalicznego i uporządkowanej sieci krystalicznej z "gazem elektronowym".
- Dzielą się na metale żelazne, nieżelazne (lekkie, ciężkie, szlachetne) oraz stopy, z których każdy ma specyficzne zastosowania.
- Są nieodzowne w budownictwie, elektronice, motoryzacji, przemyśle i przedmiotach codziennego użytku.

Czym tak naprawdę jest metal? Prosta definicja na start
Metale to pierwiastki chemiczne lub ich stopy, które charakteryzują się szeregiem specyficznych właściwości, odróżniających je od niemetali. Co ciekawe, stanowią one zdecydowaną większość pierwiastków w układzie okresowym, co świadczy o ich fundamentalnym znaczeniu w chemii i materiałoznawstwie. W temperaturze pokojowej niemal wszystkie metale występują w stanie stałym, z wyjątkiem rtęci, która jest płynna. W naturze metale rzadko występują w czystej postaci; najczęściej spotykamy je w formie rud, czyli skał zawierających związki metali, z których dopiero w procesach technologicznych pozyskuje się czysty surowiec.
Metal w oczach chemika – co mówi układ okresowy pierwiastków?
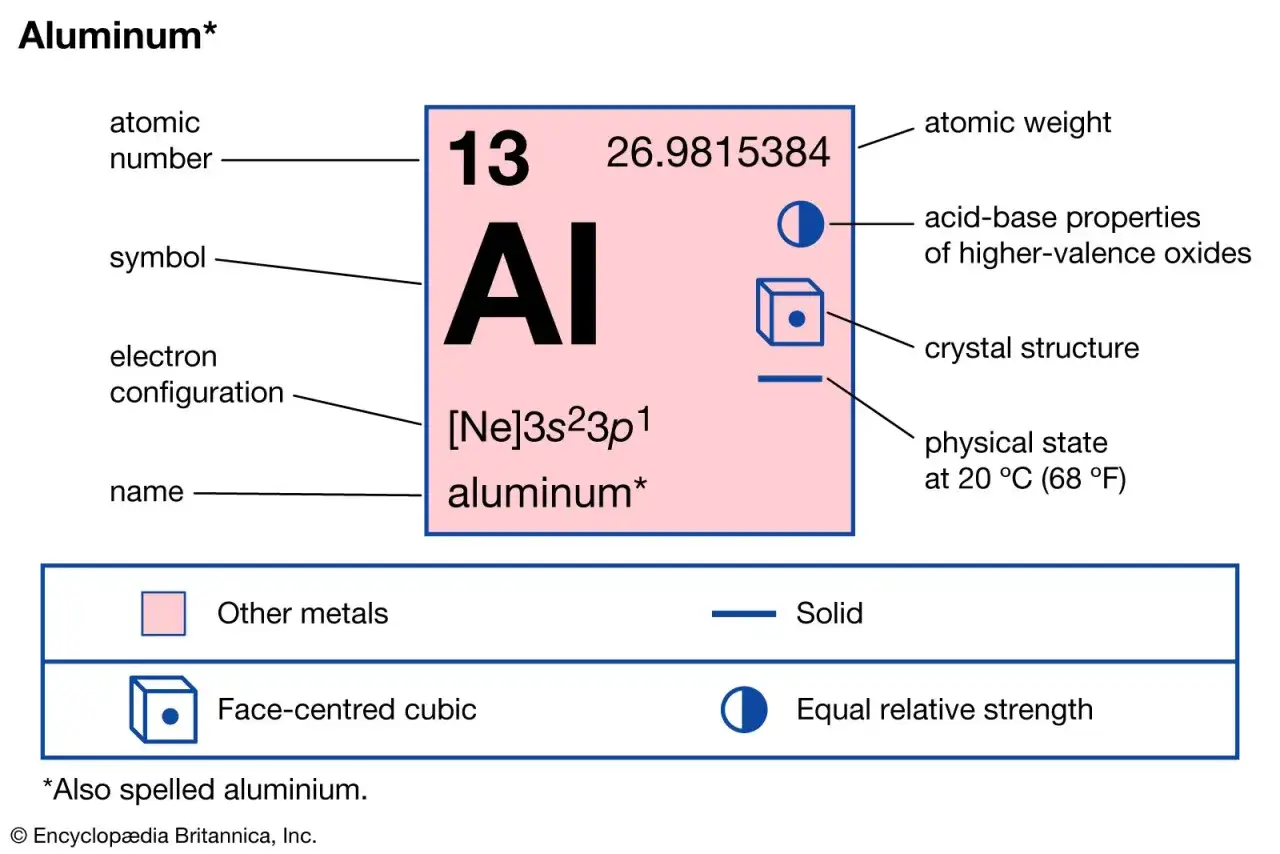
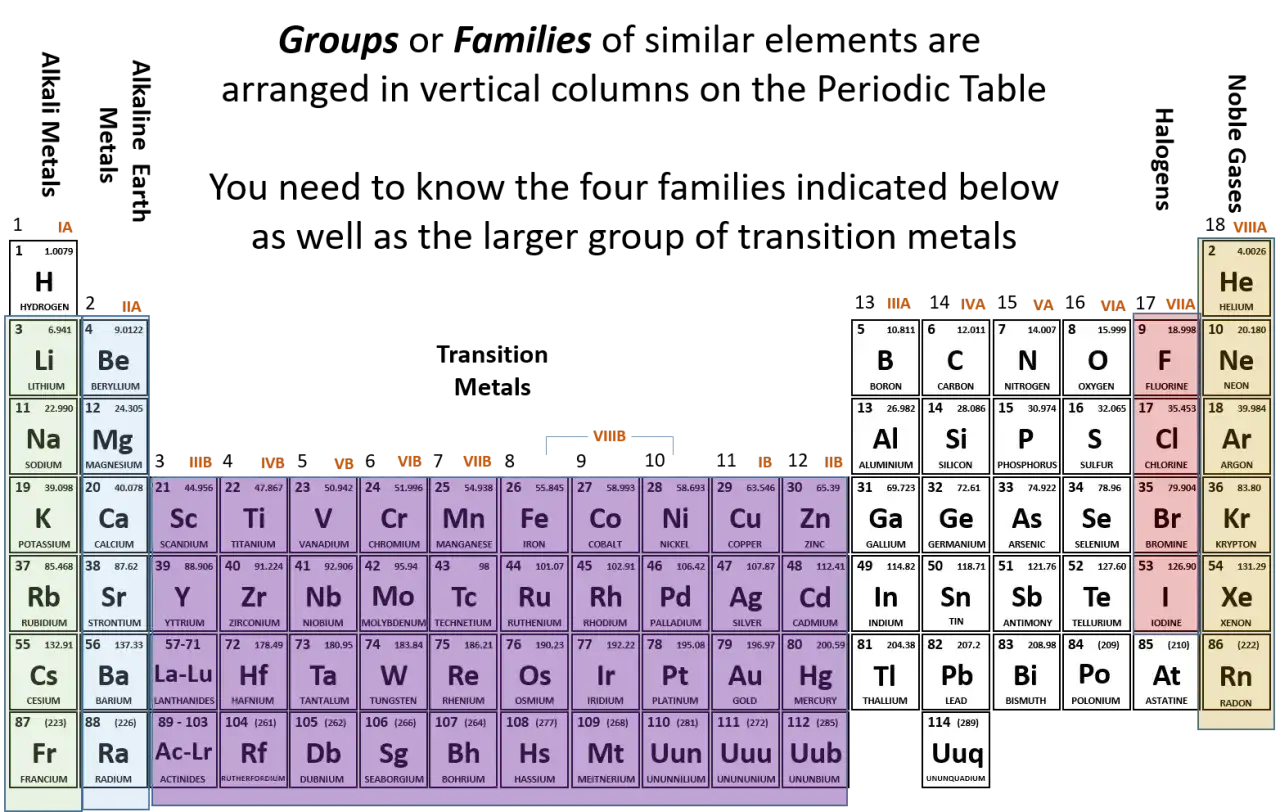
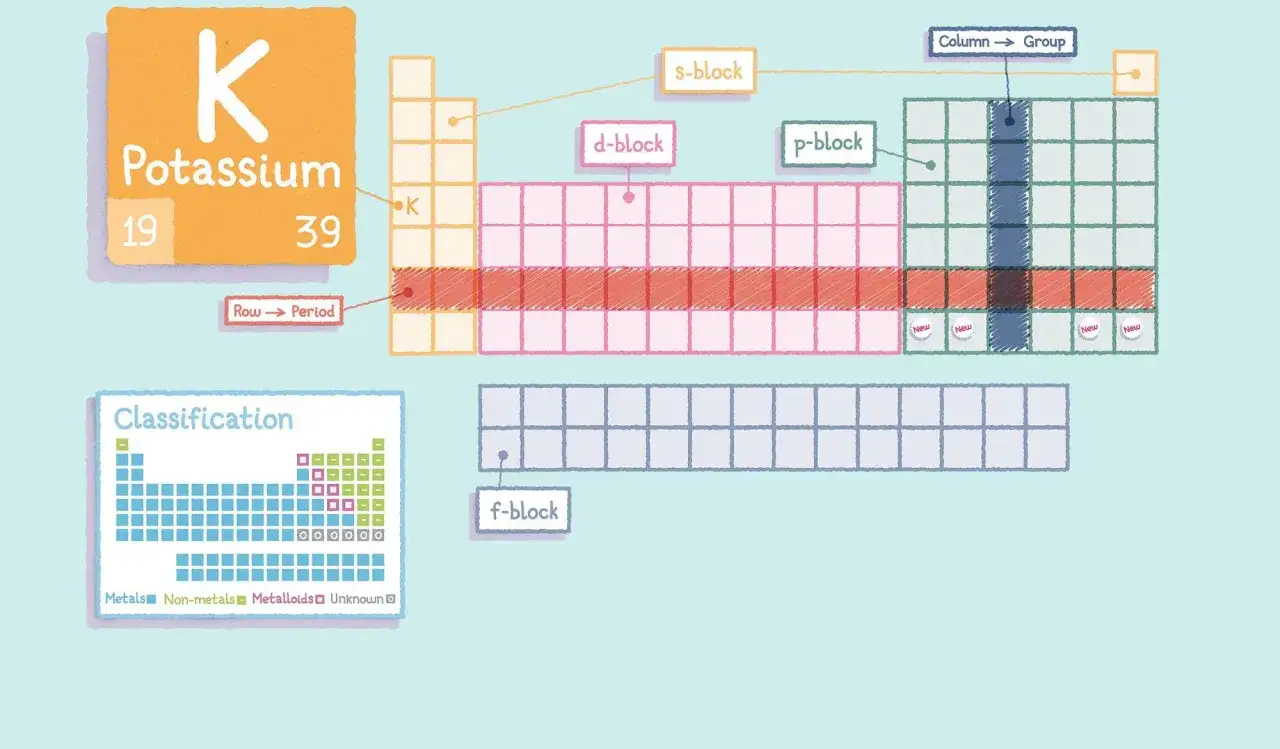
Dla chemika układ okresowy pierwiastków jest mapą, która jasno wskazuje, gdzie znajdują się metale. Zajmują one lewą i środkową część tabeli, oddzielone od niemetali linią metaloidów. Ta pozycja nie jest przypadkowa – odzwierciedla ona ich podstawowe właściwości chemiczne. Metale posiadają stosunkowo niewiele elektronów walencyjnych (elektronów na najbardziej zewnętrznej powłoce atomu), które są słabo związane z jądrem. To właśnie ta cecha sprawia, że metale mają silną tendencję do oddawania elektronów i tworzenia dodatnio naładowanych jonów, czyli kationów, co jest kluczowe dla ich reaktywności chemicznej.
Od rudy do czystego surowca – jak metale powstają w naturze?
Jak wspomniałem, metale w naturze najczęściej występują w postaci rud, czyli minerałów lub skał, z których opłacalnie można pozyskać dany metal. Proces ich wydobycia i przetworzenia, zwany metalurgią, jest niezwykle złożony i energochłonny. Obejmuje on szereg etapów, od wydobycia rudy, przez jej wzbogacanie (usuwanie zbędnych składników), aż po redukcję związków metalu do czystej postaci, często w wysokich temperaturach w piecach hutniczych. To właśnie dzięki tym procesom możemy cieszyć się czystymi metalami, które następnie formujemy i wykorzystujemy w niezliczonych zastosowaniach.
Po czym bezbłędnie rozpoznasz metal? Kluczowe właściwości fizyczne
Właściwości fizyczne metali są tym, co sprawia, że są one tak wszechstronne i łatwo rozpoznawalne w naszym otoczeniu. To właśnie one decydują o ich zastosowaniach – od elektryki po budownictwo. Przyjrzyjmy się bliżej, co sprawia, że metale są tak wyjątkowe.
Dlaczego metale przewodzą prąd i ciepło? Tajemnica swobodnych elektronów
Jedną z najbardziej charakterystycznych cech metali jest ich doskonałe przewodnictwo elektryczne i cieplne. Za tę właściwość odpowiadają tak zwane
swobodne elektrony, czyli elektrony walencyjne, które nie są trwale związane z żadnym konkretnym atomem, lecz mogą swobodnie poruszać się w całej objętości metalu. Tworzą one swoisty "gaz elektronowy". Kiedy przyłożymy napięcie elektryczne, te elektrony zaczynają się uporządkowanie przemieszczać, tworząc prąd elektryczny. Podobnie, gdy dostarczymy ciepło, swobodne elektrony szybko przekazują energię kinetyczną, rozprowadzając ciepło po całym materiale. To właśnie ta mobilność elektronów jest sekretem ich wyjątkowych zdolności przewodzenia.
Co oznacza, że metal jest kowalny i ciągliwy?
Kowalność i ciągliwość to dwie niezwykle ważne właściwości mechaniczne metali, które umożliwiają ich obróbkę i formowanie. Kowalność to zdolność metalu do trwałego odkształcania się pod wpływem uderzeń lub nacisku, bez pękania. Dzięki niej możemy kuć metale, tworząc z nich blachy czy inne płaskie elementy. Z kolei ciągliwość to zdolność do rozciągania się i wyciągania w druty bez utraty spójności. To właśnie dzięki ciągliwości miedź może być produkowana w postaci cienkich przewodów elektrycznych. Te cechy wynikają z elastyczności wiązań metalicznych i możliwości przemieszczania się atomów w sieci krystalicznej bez jej zerwania.
Zagadka metalicznego połysku – dlaczego metale błyszczą?
Charakterystyczny metaliczny połysk, który widzimy na powierzchni metali, to efekt interakcji światła ze wspomnianym już "gazem elektronowym". Kiedy światło pada na powierzchnię metalu, swobodne elektrony absorbują energię świetlną, a następnie natychmiast ją reemitują, czyli odbijają. To odbicie światła w szerokim zakresie długości fal sprawia, że metale wydają się błyszczące i nieprzezroczyste. Intensywność i barwa połysku mogą się różnić w zależności od rodzaju metalu i jego czystości, co jest widoczne na przykładzie srebra czy złota.
Stan skupienia i temperatura topnienia – czy każdy metal jest twardy?
Większość metali w temperaturze pokojowej występuje w stanie stałym, co jest typowe dla materiałów o silnych wiązaniach międzyatomowych. Wyjątkiem, jak już wspomniałem, jest rtęć, która jest płynna. Metale zazwyczaj charakteryzują się również wysokimi temperaturami topnienia, co czyni je idealnymi do zastosowań wymagających odporności na wysokie temperatury. Mają także stosunkowo dużą gęstość w porównaniu do innych materiałów. Jednakże, wbrew powszechnemu przekonaniu, nie każdy metal jest twardy. Istnieje szeroki zakres twardości – od bardzo miękkich metali alkalicznych, takich jak sód, które można kroić nożem, po niezwykle twarde metale, takie jak wolfram czy chrom, które są wykorzystywane w narzędziach tnących i elementach konstrukcyjnych.
Jak metale oddziałują ze światem? Właściwości chemiczne, które musisz znać
Poza imponującymi właściwościami fizycznymi, metale posiadają również unikalne cechy chemiczne, które decydują o ich reaktywności i sposobie, w jaki wchodzą w interakcje z innymi substancjami. Zrozumienie tych właściwości jest kluczowe dla ich prawidłowego wykorzystania i ochrony przed korozją.
Tendencja do oddawania elektronów, czyli tworzenie kationów
Jak już wspomniałem, fundamentalną chemiczną właściwością metali jest ich silna tendencja do oddawania elektronów walencyjnych. Dzieje się tak, ponieważ atomy metali dążą do osiągnięcia stabilnej konfiguracji elektronowej, zazwyczaj poprzez utratę elektronów i utworzenie dodatnio naładowanych jonów – kationów. Ta zdolność do łatwego oddawania elektronów sprawia, że metale są dobrymi reduktorami w reakcjach chemicznych i chętnie wchodzą w reakcje z niemetalami, tworząc związki jonowe. Im łatwiej metal oddaje elektrony, tym jest bardziej reaktywny chemicznie.
Reakcje z kwasami i tworzenie tlenków zasadowych
Wiele metali reaguje z kwasami, wypierając z nich wodór i tworząc sole. Na przykład, gdy wrzucimy kawałek cynku do roztworu kwasu solnego, zaobserwujemy wydzielanie się gazowego wodoru i powstanie chlorku cynku. Reaktywność metali z kwasami jest różna – niektóre reagują gwałtownie, inne bardzo powoli. Inną ważną cechą chemiczną jest to, że tlenki metali, czyli związki metali z tlenem, mają zazwyczaj charakter zasadowy. Oznacza to, że po rozpuszczeniu w wodzie tworzą zasady (np. tlenek sodu tworzy wodorotlenek sodu) lub reagują z kwasami, tworząc sole i wodę. Ta właściwość jest wykorzystywana w wielu procesach przemysłowych.
Co kryje się w środku? Budowa wewnętrzna, która wyjaśnia wszystko
Aby w pełni zrozumieć, dlaczego metale posiadają tak unikalne właściwości fizyczne i chemiczne, musimy zajrzeć do ich wnętrza, na poziom atomowy. To właśnie budowa wewnętrzna, a zwłaszcza rodzaj wiązania chemicznego i uporządkowanie atomów, jest kluczem do wyjaśnienia ich niezwykłości. Myślę, że to jeden z najbardziej fascynujących aspektów materiałoznawstwa.
Wiązanie metaliczne – klej, który łączy atomy w całość
Sercem unikalnych właściwości metali jest wiązanie metaliczne. W przeciwieństwie do wiązań kowalencyjnych czy jonowych, w wiązaniu metalicznym elektrony walencyjne nie są przypisane do konkretnych atomów. Zamiast tego, są one zdelokalizowane – tworzą swobodnie poruszającą się "chmurę elektronową" lub "gaz elektronowy", który otacza dodatnio naładowane jony metali (czyli rdzenie atomowe, składające się z jądra i elektronów wewnętrznych powłok). Wiązanie metaliczne polega na elektrostatycznym oddziaływaniu między tymi dodatnimi jonami a ujemnie naładowaną chmurą elektronów. To właśnie ten "klej" utrzymuje atomy metali razem, zapewniając jednocześnie swobodę ruchu elektronów, co jest fundamentalne dla ich przewodnictwa.
Sieć krystaliczna i "gaz elektronowy" – sekret uporządkowanej struktury
Atomy metali w stanie stałym tworzą wysoce uporządkowaną strukturę przestrzenną, zwaną siecią krystaliczną. Oznacza to, że atomy są ułożone w regularny, powtarzalny wzór. Typowe struktury krystaliczne metali to na przykład sieć regularna przestrzennie centrowana (np. żelazo), regularna ściennie centrowana (np. miedź, aluminium) czy heksagonalna gęsto upakowana (np. tytan, magnez). W tej uporządkowanej sieci, pomiędzy dodatnio naładowanymi jonami metali, przemieszcza się wspomniany już "gaz elektronowy". Ta kombinacja uporządkowanej sieci krystalicznej i swobodnych, zdelokalizowanych elektronów jest odpowiedzialna za większość charakterystycznych właściwości metali: od doskonałego przewodnictwa elektrycznego i cieplnego, poprzez metaliczny połysk, aż po kowalność i ciągliwość. Możliwość przemieszczania się atomów w sieci bez zerwania wiązań, dzięki elastyczności "gazu elektronowego", pozwala na odkształcanie metali bez ich pękania.
Jak odróżnić metale od siebie? Najważniejsze rodzaje i podziały
Chociaż metale mają wiele wspólnych cech, ich różnorodność jest ogromna. Od lekkiego aluminium po ciężki ołów, od stali po złoto – każdy metal i stop ma swoje unikalne właściwości i zastosowania. Klasyfikacja metali pomaga nam uporządkować tę różnorodność i zrozumieć, dlaczego dany materiał jest wykorzystywany w konkretnym celu. Według danych Wikipedia, istnieje wiele sposobów klasyfikacji metali, ale najczęściej spotykane opierają się na ich składzie chemicznym i właściwościach.
| Rodzaj Metalu/Stopu | Główny Składnik/Charakterystyka | Przykłady | Kluczowe Zastosowania |
|---|---|---|---|
| Metale żelazne | Głównym składnikiem jest żelazo; magnetyczne, podatne na korozję (bez zabezpieczeń) | Stal (węglowa, nierdzewna), żeliwo | Budownictwo, maszyny, motoryzacja, narzędzia |
| Metale nieżelazne lekkie | Niska gęstość, wysoka wytrzymałość w stosunku do masy, często odporne na korozję | Aluminium, tytan, magnez | Lotnictwo, motoryzacja, sprzęt sportowy, elektronika |
| Metale nieżelazne ciężkie | Wysoka gęstość, dobre przewodnictwo, różna odporność na korozję | Miedź, cynk, ołów, nikiel | Przewody elektryczne, pokrycia dachowe, baterie, stopy (mosiądz, brąz) |
| Metale szlachetne | Wysoka odporność na korozję i utlenianie, rzadkie, cenne | Złoto, srebro, platyna, pallad | Biżuteria, elektronika (styki), katalizatory, inwestycje |
| Stopy metali | Mieszaniny dwóch lub więcej metali (lub metalu z niemetalem), poprawiające właściwości | Brąz (miedź+cyna), mosiądz (miedź+cynk), duraluminium (aluminium+miedź+magnez) | Narzędzia, instrumenty muzyczne, elementy konstrukcyjne, monety |
Metale żelazne – kręgosłup przemysłu (stal, żeliwo)
Metale żelazne to grupa materiałów, w których głównym składnikiem jest żelazo. Są one absolutnym kręgosłupem współczesnego przemysłu i budownictwa. Najważniejszymi przedstawicielami tej grupy są stal i żeliwo. Stal to stop żelaza z węglem (do 2%), często z dodatkiem innych pierwiastków stopowych, które poprawiają jej właściwości, np. stal nierdzewna zawiera chrom i nikiel. Żeliwo natomiast to stop żelaza z węglem (powyżej 2%). Metale żelazne charakteryzują się wysoką wytrzymałością mechaniczną i są stosunkowo tanie w produkcji, co sprawia, że są niezastąpione w konstrukcjach budowlanych, produkcji maszyn, pojazdów czy narzędzi. Ich wadą jest podatność na korozję, jeśli nie są odpowiednio zabezpieczone.Metale nieżelazne (kolorowe) – od lekkiego aluminium po ciężki ołów
Metale nieżelazne, często nazywane również metalami kolorowymi, to wszystkie metale i ich stopy, które nie zawierają żelaza jako głównego składnika. Ta grupa jest niezwykle zróżnicowana i dzieli się na kilka podkategorii. Wyróżniamy metale lekkie, takie jak aluminium, tytan czy magnez, które charakteryzują się niską gęstością i często wysoką wytrzymałością w stosunku do masy, co czyni je idealnymi do zastosowań w lotnictwie i motoryzacji. Z drugiej strony mamy metale ciężkie, do których należą miedź, cynk, ołów czy nikiel. Są one gęstsze, a ich właściwości są bardzo różnorodne – miedź jest doskonałym przewodnikiem, cynk chroni stal przed korozją, a ołów jest wykorzystywany m.in. w akumulatorach. Metale nieżelazne często cechuje lepsza odporność na korozję niż metale żelazne.
Metale szlachetne – dlaczego złoto i platyna są tak cenne?
Metale szlachetne to specyficzna grupa metali nieżelaznych, do której zaliczamy złoto, srebro, platynę i pallad. Ich wyjątkowa wartość wynika z dwóch głównych cech: rzadkości występowania w naturze oraz niezwykłej odporności na korozję i utlenianie. Oznacza to, że nie rdzewieją, nie matowieją i nie wchodzą łatwo w reakcje z innymi substancjami, co sprawia, że zachowują swój blask i właściwości przez bardzo długi czas. Te cechy sprawiają, że są one cenione nie tylko w jubilerstwie, ale także w elektronice (np. w stykach), medycynie czy jako katalizatory w przemyśle chemicznym.
Czym są stopy metali i dlaczego są tak popularne (np. brąz, mosiądz)?
Czyste metale, choć mają wiele zalet, często nie posiadają wszystkich pożądanych właściwości dla konkretnych zastosowań. Tutaj z pomocą przychodzą stopy metali, czyli mieszaniny dwóch lub więcej metali, lub metalu z niemetalem. Celem tworzenia stopów jest poprawa właściwości czystych metali, takich jak twardość, wytrzymałość, odporność na korozję czy temperatura topnienia. Klasycznymi przykładami są brąz (stop miedzi z cyną), który jest twardszy i bardziej odporny na korozję niż czysta miedź, oraz mosiądz (stop miedzi z cynkiem), ceniony za swoje właściwości akustyczne i łatwość obróbki. Stopy są wszechobecne w naszym życiu, od narzędzi i elementów konstrukcyjnych, po monety i instrumenty muzyczne, oferując inżynierom i projektantom szerokie spektrum materiałów o dostosowanych właściwościach.
Od drapaczy chmur po smartfony – gdzie na co dzień spotykasz metale?
Metale są tak głęboko zakorzenione w naszej cywilizacji, że często nawet nie zdajemy sobie sprawy z ich wszechobecności. Od monumentalnych konstrukcji po mikroskopijne komponenty w naszych kieszeniach, metale odgrywają niezastąpioną rolę, umożliwiając rozwój technologii i poprawiając jakość naszego życia. To naprawdę fascynujące, jak wiele zawdzięczamy tym materiałom.
Zastosowanie w budownictwie i przemyśle ciężkim
W budownictwie metale są absolutnym fundamentem. Konstrukcje stalowe stanowią szkielet wieżowców, mostów, hal produkcyjnych i stadionów, zapewniając im wytrzymałość i stabilność. Żelazo i stal są wykorzystywane do produkcji prętów zbrojeniowych w betonie, zwiększając jego odporność na rozciąganie. W przemyśle ciężkim metale są niezbędne do budowy maszyn, urządzeń, statków, pociągów i rurociągów. Ich wytrzymałość, odporność na zużycie i zdolność do pracy w ekstremalnych warunkach sprawiają, że są niezastąpione w sektorach takich jak górnictwo, energetyka czy transport.
Rola metali w nowoczesnej elektronice i technologii
W dzisiejszej erze cyfrowej metale odgrywają kluczową rolę w elektronice i nowoczesnych technologiach. Miedź jest podstawowym materiałem na przewody elektryczne ze względu na swoje doskonałe przewodnictwo. W naszych smartfonach, komputerach i innych urządzeniach elektronicznych znajdziemy śladowe ilości złota i srebra w stykach i złączach, co zapewnia niezawodność i efektywność przesyłu sygnałów. Aluminium i tytan, dzięki swojej lekkości i wytrzymałości, są szeroko stosowane w przemyśle lotniczym i motoryzacyjnym, zwłaszcza w samochodach elektrycznych, gdzie redukcja masy jest kluczowa dla zasięgu i wydajności. Bez metali rozwój współczesnej technologii byłby niemożliwy.
Przeczytaj również: Blacha żaluzjowa - kompletny przewodnik po wyborze i montażu
Metale w przedmiotach codziennego użytku – od kuchni po biżuterię
Wystarczy rozejrzeć się wokół, by dostrzec metale w niezliczonych przedmiotach codziennego użytku. W kuchni używamy naczyń ze stali nierdzewnej, sztućców, aluminiowych folii. Nasze narzędzia, takie jak młotki, klucze czy śrubokręty, wykonane są ze stali. Monety w naszych portfelach to stopy metali, a zamki i klucze zapewniają bezpieczeństwo. Wreszcie, metale szlachetne, takie jak złoto i srebro, od wieków są wykorzystywane do tworzenia biżuterii, symbolizując piękno i wartość. Nawet w naszych rowerach, sprzęcie sportowym czy elementach mebli znajdziemy metale, które zapewniają im funkcjonalność i trwałość.

