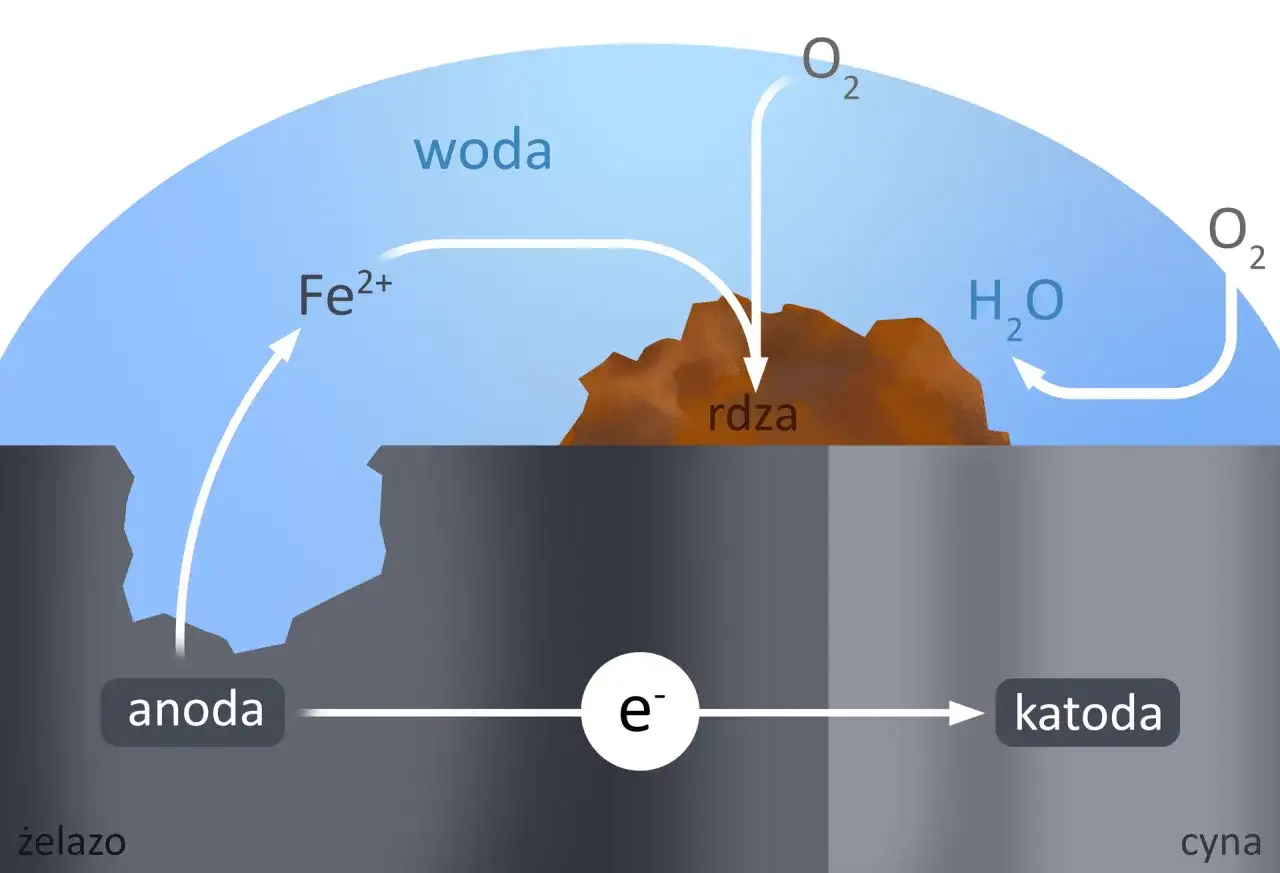
Korozja elektrochemiczna to niszczenie metali w wyniku reakcji chemicznych i elektrycznych
- Proces korozji elektrochemicznej zachodzi w wyniku powstania mikroogniw galwanicznych na powierzchni metalu.
- Do jej wystąpienia niezbędne są trzy elementy: anoda, katoda oraz elektrolit.
- Elektrolitem najczęściej jest woda z rozpuszczonymi gazami (tlen, dwutlenek węgla) lub solami.
- Przykłady korozji obejmują korozję galwaniczną, szczelinową, wżerową i naprężeniową.
- Czynniki takie jak wilgotność, sole, zanieczyszczenia i temperatura przyspieszają proces niszczenia.
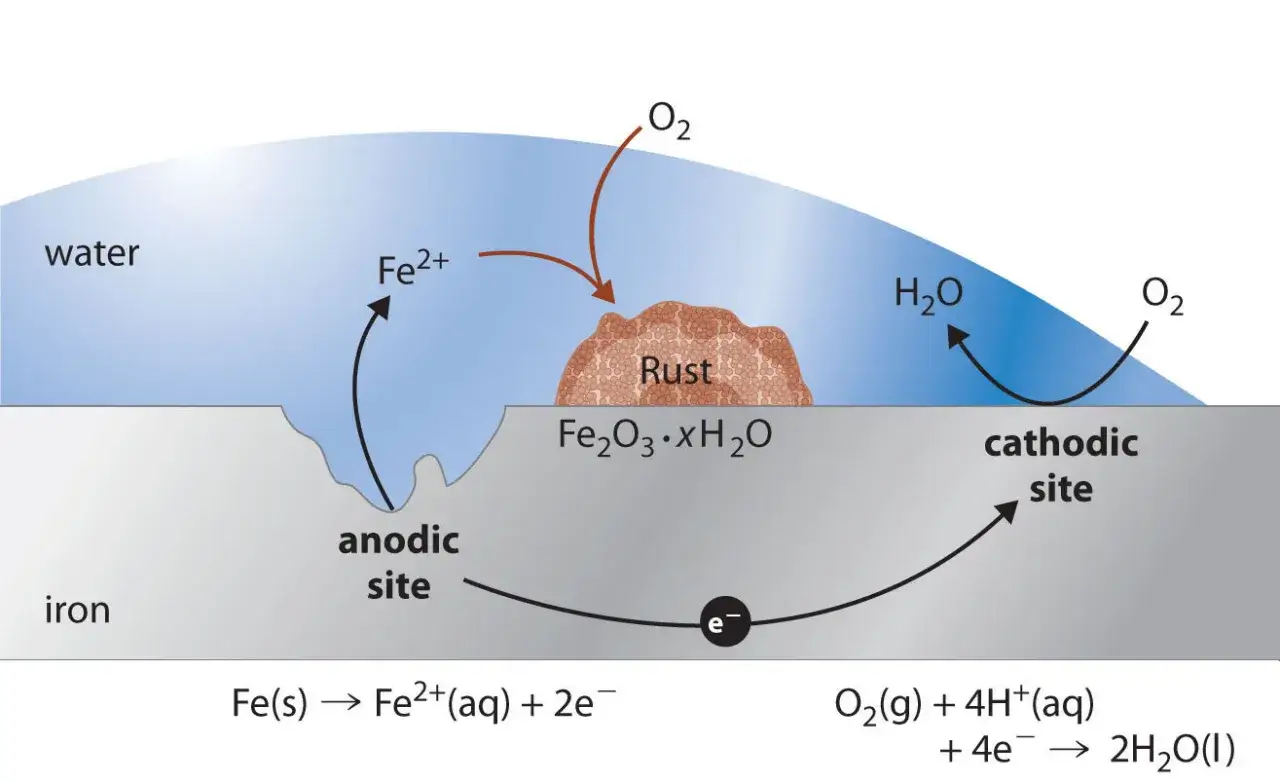
Dlaczego metalowe elementy niszczeją? Poznaj mechanizm korozji elektrochemicznej
Korozja elektrochemiczna to nic innego jak niszczenie metali w wyniku reakcji chemicznych i elektrycznych. Proces ten zachodzi, gdy na powierzchni metalu tworzą się tak zwane mikroogniwa galwaniczne. W praktyce oznacza to, że metal zaczyna "rozpuszczać się" w środowisku, tracąc swoje właściwości i strukturę. Z moich obserwacji wynika, że zrozumienie tego podstawowego mechanizmu jest kluczowe do skutecznego zapobiegania uszkodzeniom.
Anoda, katoda i elektrolit – Trzy elementy niezbędne do powstania rdzy
Aby korozja elektrochemiczna mogła w ogóle zaistnieć, muszą być spełnione trzy podstawowe warunki, czyli muszą współistnieć trzy kluczowe elementy: anoda, katoda i elektrolit. Anoda to miejsce, w którym metal ulega utlenianiu, czyli „oddaje” elektrony i przechodzi w formę jonową, co jest równoznaczne z jego niszczeniem. Katoda natomiast to obszar, gdzie zachodzi redukcja, czyli elektrony są przyjmowane przez inne substancje, najczęściej tlen. Pomiędzy anodą a katodą musi istnieć ścieżka dla przepływu elektronów (sam metal) oraz elektrolit – środowisko przewodzące prąd, które umożliwia transport jonów i zamyka obwód elektryczny. Bez jednego z tych elementów korozja elektrochemiczna nie będzie postępować.
Jak woda i powietrze tworzą idealne warunki do niszczenia metali?
Woda i powietrze, choć wydają się nieszkodliwe, są często głównymi winowajcami korozji. Woda, zwłaszcza gdy zawiera rozpuszczone gazy takie jak tlen czy dwutlenek węgla, staje się doskonałym elektrolitem. Cząsteczki tlenu z powietrza działają jako utleniacz, przyjmując elektrony na powierzchni katody. W ten sposób powstaje idealne środowisko dla tworzenia się ogniw korozyjnych. Woda zapewnia medium dla ruchu jonów, a tlen napędza reakcję, co w efekcie prowadzi do systematycznego niszczenia metalu. To właśnie dlatego wilgotne powietrze jest tak agresywne dla wielu metalowych konstrukcji. Przejdźmy teraz do konkretnych przykładów, które najlepiej ilustrują te mechanizmy.
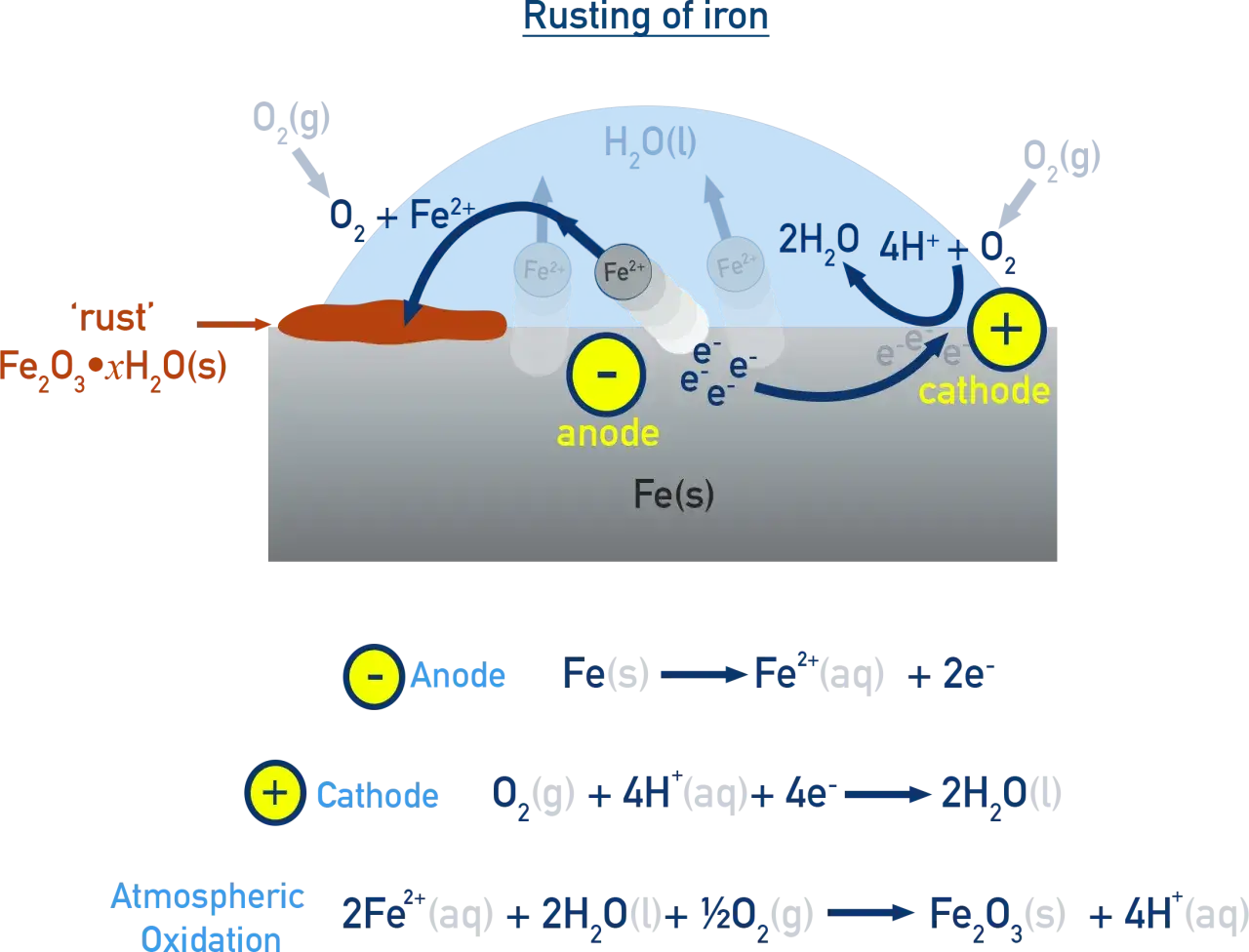
Korozja elektrochemiczna w praktyce: Przykłady, które widzisz na co dzień
Zjawisko korozji elektrochemicznej otacza nas wszędzie, choć nie zawsze zdajemy sobie z tego sprawę. Od rdzy na starym samochodzie po uszkodzone połączenia w instalacjach – wszędzie tam, gdzie metale stykają się z wilgocią i różnymi substancjami, mogą zachodzić te niszczące procesy. Przyjrzyjmy się kilku typowym sytuacjom.Rdza na karoserii samochodu – Dlaczego zimą problem się nasila?
Jednym z najbardziej powszechnych przykładów jest rdza na karoserii samochodu. Zimą problem ten staje się szczególnie dotkliwy. Sól drogowa, używana do rozmrażania nawierzchni, w połączeniu z wilgocią tworzy silny elektrolit. Uszkodzenia lakieru, rysy czy odpryski odsłaniają metalową stal, która w kontakcie z solanką i tlenem z powietrza zaczyna korodować. Często zdarza się, że karoseria jest pokryta warstwą cynku (ocynkowana), która ma ją chronić. Jednak gdy ta warstwa zostanie uszkodzona, powstaje ogniwo galwaniczne między stalą a resztkami cynku, gdzie cynk (mniej szlachetny) poświęca się, chroniąc stal. Niestety, gdy cynk się wyczerpie, stal staje się bezbronna. Różnice w metalach, a nawet naprężenia w samej karoserii, mogą tworzyć mikroogniwa, przyspieszając proces niszczenia. Zima, z jej wilgocią i solą, jest więc prawdziwym testem dla powłok ochronnych samochodu.
Połączenie miedzi i stali w instalacji C. O. – Kto kogo niszczy?
Problem korozji galwanicznej jest doskonale widoczny w instalacjach centralnego ogrzewania, gdzie często spotykamy połączenia miedzi i stali. Miedź jest metalem szlachetniejszym niż stal. Kiedy te dwa metale stykają się ze sobą w obecności wody (która działa jako elektrolit w instalacji), powstaje ogniwo galwaniczne. Zgodnie z tym, co wskazują dane Wikipedii na temat korozji galwanicznej, metal mniej szlachetny, czyli w tym przypadku stal, staje się anodą i ulega przyspieszonej korozji. Widziałem wiele przypadków, gdzie stalowe śruby użyte do mocowania miedzianych elementów w instalacjach wodnych ulegały szybkiemu zniszczeniu, podczas gdy miedź pozostawała nienaruszona. To klasyczny przykład, jak niewłaściwe połączenie materiałów prowadzi do nieodwracalnych uszkodzeń.
Korozja pod uszczelką w pralce – Wróg ukryty w szczelinach
Korozja nie zawsze jest widoczna na pierwszy rzut oka. Czasami ukrywa się w ciasnych zakamarkach, gdzie dostęp tlenu jest ograniczony. Doskonałym przykładem jest korozja szczelinowa, która może pojawić się pod uszczelką w pralce. Woda z detergentami, która gromadzi się w szczelinie między uszczelką a metalowym bębnem, działa jako elektrolit. Wewnątrz szczeliny dostęp tlenu jest utrudniony, co prowadzi do powstania różnicy w stężeniu tlenu w porównaniu do zewnętrznej, dobrze napowietrzonej powierzchni. Obszar o niższym stężeniu tlenu (w szczelinie) staje się anodą i ulega korozji, podczas gdy obszar zewnętrzny staje się katodą. W efekcie metal pod uszczelką zaczyna niszczeć, co z czasem może prowadzić do przecieków i poważniejszych awarii.
Niszczenie stalowego ogrodzenia na styku z betonową podmurówką
Stalowe ogrodzenia często są osadzane w betonowych podmurówkach, co wydaje się solidnym rozwiązaniem. Jednak na styku stali i betonu może dochodzić do korozji. Wilgoć, która zatrzymuje się w tej szczelinie, tworzy elektrolit. W zależności od składu betonu i warunków środowiskowych, może to być przykład korozji galwanicznej (jeśli beton zawiera składniki, które reagują z metalem i tworzą różnicę potencjałów) lub częściej korozji różnicowej napowietrzania, czyli odmiany korozji szczelinowej. Beton, choć pozornie suchy, często jest porowaty i może utrzymywać wilgoć, tworząc idealne warunki dla rozwoju ognisk korozyjnych w miejscu styku z metalem.
Baterie i "wylane" ogniwa – Korozja, która daje energię
Paradoksalnie, działanie baterii to nic innego jak kontrolowany proces elektrochemiczny, który wykorzystujemy do pozyskiwania energii. Wewnątrz baterii zachodzą reakcje utleniania i redukcji, które generują prąd. Jednak gdy bateria się zużyje lub zostanie uszkodzona, często obserwujemy zjawisko "wylania" ogniwa. To, co widzimy jako biały, krystaliczny nalot, to produkty reakcji elektrochemicznych, które wydostały się na zewnątrz. Jest to forma korozji, która w tym przypadku dotyczy nie samego metalu obudowy, ale substancji chemicznych wewnątrz baterii, które, wydostając się, mogą niszczyć otoczenie, np. styki w urządzeniach elektronicznych. To przypomina nam, że elektrochemia ma swoje jasne i ciemne strony.
Nie każda rdza jest taka sama: Jakie są kluczowe rodzaje korozji elektrochemicznej?
Choć potocznie mówimy o "rdzy", procesy korozyjne mogą przybierać różne formy, w zależności od warunków środowiskowych i rodzaju metalu. Zrozumienie tych różnic jest kluczowe dla właściwej diagnostyki i wyboru metod ochrony. Poznajmy najważniejsze typy korozji elektrochemicznej.
Korozja galwaniczna – Gdy spotykają się dwa różne metale
Jak już wspomniałem, korozja galwaniczna, zwana również kontaktową, występuje, gdy dwa różne metale, o odmiennych potencjałach elektrochemicznych, stykają się ze sobą w obecności elektrolitu. Metal mniej szlachetny (czyli ten o niższym potencjale), staje się anodą i ulega przyspieszonej korozji, "poświęcając się" dla metalu szlachetniejszego. Jest to zjawisko, które musimy brać pod uwagę przy projektowaniu wszelkich konstrukcji, gdzie łączone są różne metale, aby uniknąć niepożądanych uszkodzeń.
Korozja wżerowa – Ciche drążenie głębokich ubytków w metalu
Korozja wżerowa to szczególnie podstępna forma korozji, ponieważ prowadzi do powstawania małych, ale bardzo głębokich ubytków, często trudnych do wykrycia na wczesnym etapie. Zaczyna się od niewielkiego uszkodzenia warstwy pasywnej metalu (np. tlenkowej), a następnie rozwija się w głąb materiału. Jest często inicjowana przez jony chlorkowe (Cl-), dlatego stanowi poważny problem w środowiskach morskich, w kontakcie z solanką czy w basenach. Jej niebezpieczeństwo polega na tym, że może prowadzić do perforacji materiału, nawet jeśli ogólna utrata masy metalu jest niewielka.
Korozja szczelinowa – Problem ciasnych i wilgotnych przestrzeni
Korozja szczelinowa, którą już omawiałem na przykładzie pralki, rozwija się w wąskich szczelinach i zakamarkach, gdzie dostęp tlenu jest ograniczony. W takich miejscach, na skutek różnicy w stężeniu tlenu, tworzy się ogniwo korozyjne. Obszar o niższym stężeniu tlenu staje się anodą i koroduje. Problem ten dotyczy często połączeń śrubowych, nitowanych, pod uszczelkami czy w miejscach styku dwóch powierzchni, które nie są idealnie dopasowane. To pokazuje, jak ważne jest precyzyjne wykonanie i odpowiednie uszczelnienie konstrukcji.Korozja naprężeniowa – Kiedy naprężenie materiału spotyka agresywne środowisko
Korozja naprężeniowa to złożone zjawisko, które występuje, gdy metal jest jednocześnie poddany działaniu środowiska korozyjnego i naprężeń rozciągających. Naprężenia te mogą być wynikiem obciążenia zewnętrznego lub wewnętrznych naprężeń technologicznych (np. po spawaniu, obróbce plastycznej). W połączeniu z agresywnym środowiskiem, naprężenia te prowadzą do powstawania pęknięć, które rozprzestrzeniają się w materiale, często bez widocznych oznak ogólnej korozji. Jest to szczególnie niebezpieczne, ponieważ może prowadzić do nagłych i katastrofalnych awarii konstrukcji, nawet przy niewielkiej utracie masy metalu. Z mojego doświadczenia wynika, że ten rodzaj korozji wymaga szczególnej uwagi w przemyśle.
Co sprawia, że metale korodują szybciej? Najważniejsze czynniki ryzyka
Szybkość, z jaką metale ulegają korozji elektrochemicznej, nie jest stała. Zależy od wielu czynników środowiskowych i materiałowych. Zrozumienie tych czynników pozwala na lepsze przewidywanie i zapobieganie degradacji materiałów. Przyjrzyjmy się najważniejszym z nich.
Wpływ wilgoci i soli – Zabójczy duet dla stali i żelaza
Wilgoć i sole tworzą duet, który jest wyjątkowo zabójczy dla wielu metali, zwłaszcza dla stali i żelaza. Wysoka wilgotność dostarcza niezbędnego elektrolitu, umożliwiając przepływ jonów. Obecność soli, zwłaszcza chlorków (takich jak sól drogowa czy sól morska), znacząco zwiększa przewodnictwo elektryczne elektrolitu. Im lepsze przewodnictwo, tym szybciej elektrony mogą przepływać między anodą a katodą, co bezpośrednio przekłada się na znacznie przyspieszone reakcje korozyjne. Dlatego środowisko morskie czy obszary, gdzie często używa się soli do odladzania, są szczególnie agresywne dla metalowych konstrukcji.
Zanieczyszczenia powietrza (smog) jako katalizator procesów korozyjnych
Nie tylko wilgoć i sole, ale również zanieczyszczenia powietrza, takie jak smog przemysłowy, odgrywają znaczącą rolę w przyspieszaniu korozji. Tlenki siarki (SOx) i tlenki azotu (NOx), emitowane przez przemysł i transport, rozpuszczają się w wodzie deszczowej, tworząc kwaśne deszcze. Te kwaśne opady obniżają pH elektrolitu (wody na powierzchni metalu), co zwiększa jego agresywność i zdolność do rozpuszczania metali. W efekcie, metale w obszarach o wysokim zanieczyszczeniu powietrza korodują znacznie szybciej niż w czystych środowiskach, co jest poważnym problemem dla infrastruktury miejskiej i zabytków.
Rola temperatury – Czy ciepło zawsze przyspiesza rdzewienie?
Zazwyczaj podwyższona temperatura przyspiesza większość reakcji chemicznych, a procesy korozyjne nie są wyjątkiem. Wzrost temperatury zwiększa kinetykę reakcji anodowych i katodowych, co oznacza, że elektrony i jony poruszają się szybciej, a reakcje zachodzą z większą intensywnością. Dlatego w ciepłych środowiskach korozja często postępuje szybciej. Jednak należy pamiętać, że w niektórych specyficznych przypadkach bardzo wysoka temperatura może prowadzić do tworzenia stabilnych warstw tlenkowych, które paradoksalnie mogą chronić metal. Mimo to, w większości typowych scenariuszy, ciepło jest sprzymierzeńcem korozji. Znając te czynniki ryzyka, możemy przejść do metod, które pozwalają nam skutecznie walczyć z tym niszczącym zjawiskiem.
Jak skutecznie zatrzymać proces korozji? Sprawdzone metody ochrony metali
Skoro wiemy już, czym jest korozja elektrochemiczna i co ją przyspiesza, naturalnym krokiem jest zastanowienie się, jak możemy chronić metale przed jej niszczącym działaniem. Na szczęście, inżynieria materiałowa i chemia oferują szereg skutecznych metod, które pozwalają znacznie spowolnić, a nawet całkowicie zatrzymać ten proces.
Powłoki ochronne – od farb po cynkowanie
Jedną z najprostszych i najczęściej stosowanych metod ochrony jest izolowanie metalu od środowiska korozyjnego za pomocą powłok ochronnych. Mogą to być organiczne powłoki, takie jak farby i lakiery, które tworzą fizyczną barierę, uniemożliwiając kontakt metalu z elektrolitem i tlenem. Innym, bardzo skutecznym rozwiązaniem są powłoki metaliczne, na przykład cynkowanie, niklowanie czy chromowanie. Cynkowanie, znane także jako galwanizowanie, polega na pokryciu stali warstwą cynku. Cynk, będąc metalem mniej szlachetnym niż stal, pełni rolę anody protektorowej – to on koroduje w pierwszej kolejności, chroniąc stal. Niklowanie i chromowanie natomiast tworzą twarde, odporne na ścieranie i estetyczne warstwy, które również izolują metal od czynników korozyjnych.
Ochrona katodowa – jak "poświęcić" jeden metal, by uratować drugi?
Ochrona katodowa to zaawansowana technika, która polega na uczynieniu chronionego metalu katodą ogniwa elektrochemicznego, co zapobiega jego korozji. Można to osiągnąć na dwa sposoby. Pierwsza metoda to zastosowanie anod protektorowych (sacrificial anodes). Polega ona na połączeniu chronionego metalu z innym, mniej szlachetnym metalem (np. magnezem, cynkiem, aluminium), który będzie korodował zamiast chronionego elementu. To on "poświęca się" dla ratowania cenniejszej konstrukcji. Ta metoda jest powszechnie stosowana do ochrony kadłubów statków, rurociągów czy zbiorników podziemnych. Druga metoda to ochrona z zewnętrznym źródłem prądu (impressed current), gdzie prąd elektryczny jest dostarczany z zewnątrz, aby wymusić przepływ elektronów w kierunku chronionej konstrukcji, czyniąc ją katodą. Jest to rozwiązanie stosowane na przykład w dużych rurociągach czy platformach wiertniczych.
Przeczytaj również: Programowanie maszyn CNC - Jak zacząć i ile zarobisz?
Wybór odpowiednich materiałów i unikanie ryzykownych połączeń
Najlepszą obroną jest często prewencja, a w przypadku korozji oznacza to świadomy wybór materiałów. Stosowanie materiałów z natury odpornych na korozję, takich jak stale nierdzewne, aluminium, tytan czy tworzywa sztuczne, może całkowicie wyeliminować problem. Stale nierdzewne zawdzięczają swoją odporność warstwie pasywnej tlenku chromu, która samoczynnie się regeneruje. Równie ważne jest unikanie tworzenia ogniw galwanicznych poprzez łączenie metali o znacznie różnym potencjale elektrochemicznym w obecności elektrolitu. Jeśli takie połączenia są nieuniknione, należy zastosować izolatory elektryczne między metalami lub powłoki ochronne. Moje doświadczenie pokazuje, że już na etapie projektowania należy dokładnie analizować środowisko pracy i dobierać materiały w taki sposób, aby minimalizować ryzyko korozji.